Las agencias regulatorias de la región siguen con su escalada de aprobaciones de vacunas contra el coronavirus. La que pegó primero fue la COFEPRIS de México que dio la voz de largada cuando avaló a mediados de diciembre el uso de emergencia de la vacuna de Pfizer. Mientras que con la vacuna de AZ/Oxford la que hizo punta fue la ANMAT.
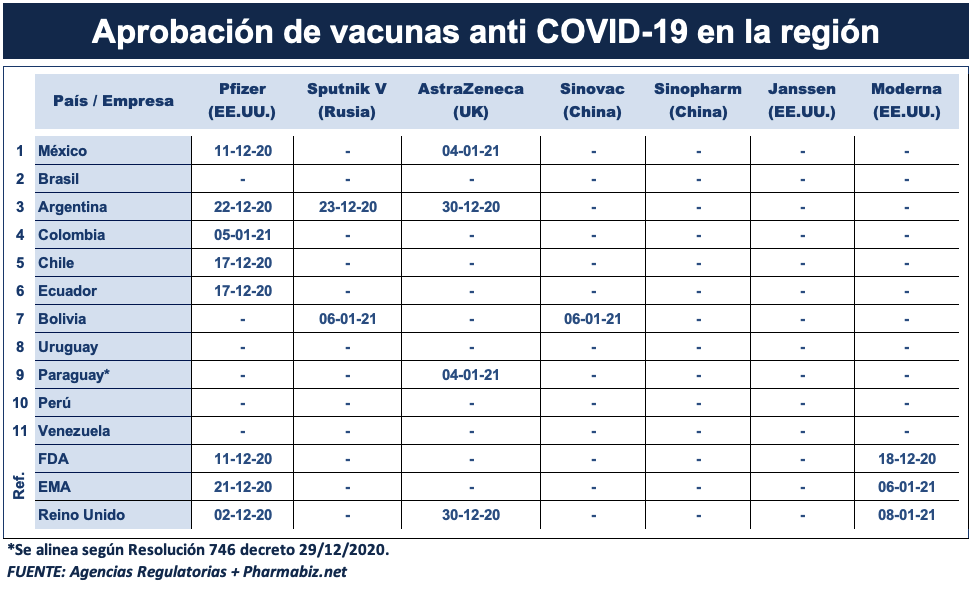
América Latina tiene su propio cronograma de aprobaciones para las vacunas anti COVID-19. En este contexto, las principales agencias regulatorias se están sacando chispas para marcar terreno y reposicionarse como referentes regionales. Ver cuadro debajo
La primera que levantó la mano fue México, el viernes 11 de diciembre de 2020 cuando autorizó el uso de emergencia de la vacuna de Pfizer-BioNTech. Esto sucedió nueve días después de que se registrara el primer aval global que corrió por cuenta del Reino Unido el miércoles 2 de diciembre. Ver artículo UK. Ver artículo COFEPRIS.
A pesar de que la ANVISA es uno de los reguladores de medicamentos referentes en la región, al momento no lleva autorizada ninguna vacuna anti COVID-19. Aunque, según las estimaciones, la primera en tener el visto bueno sería la vacuna de la china Sinovac, que hoy viernes -por medio del Instituto Butantan– elevó su solicitud de registro. Otra que podría hacerle llegar su pedido en breve es la británica AstraZeneca a través de la fundación Fiocruz.
El que también quiso diferenciarse fue el Instituto de Salud Pública (ISP) de Chile, que a pesar de ser una agencia de pequeña envergadura se le adelantó a la Argentina al darle el OK a la vacuna de Pfizer el jueves 17 de diciembre. Pocas horas después la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria de Ecuador también le concedió el visto bueno. Ver artículo.
Luego y al filo de las campanadas de Navidad -el martes 22 de diciembre- la ANMAT comandada por Manuel Limeres, oficializó la aprobación de emergencia de la vacuna de Pfizer. Por último, durante esta semana, el martes 5 de enero, la vacuna del laboratorio norteamericano recibió también la autorización de emergencia por parte del INVIMA de Colombia, por el término de un año. Ver artículo Ver artículo
Colombia, en tanto, tiene anotada a la fecha una sola aprobación con el sello del INVIMA. La agencia regulatoria respaldó esta semana la vacuna de Pfizer y BioNTech. Mientras que -al igual que Brasil– hay otros países de América Latina que todavía no le dieron el visto bueno a ninguna vacuna anti COVID-19. En el listado figuran los mercados de Paraguay; Perú; y Uruguay.
Y a pesar de que Pfizer hizo punta a nivel global, la vacuna de la británica AstraZeneca y la Universidad de Oxford, resulta mucho más relevante para Latam. Esto en función del acuerdo sellado entre varias naciones de la región y la fundación Slim. Fue así que la ANMAT marcó la cancha dándole el visto bueno al producto pocas horas después de que lo hiciera la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) de Gran Bretaña. Fue el miércoles 30 de diciembre y a pocas horas de que se dé por clausurado el 2020. Ver artículo.
Se trata de una vacuna estratégica para América Latina ya que su componente activo se fabricará en la Argentina bajo el paraguas del laboratorio mAbxience, de Hugo Sigman. El proceso de empaque se completará en México en el laboratorio mexicano Liomont. Y desde el país azteca será distribuida a toda la región, con excepción de Brasil.
El segundo país de la región que respaldó la vacuna de AstraZeneca y Oxford fue justamente México. El aval llegó desde la COFEPRIS y se registró el primer día hábil de este 2021, el pasado lunes 4 de enero. Ver artículo.
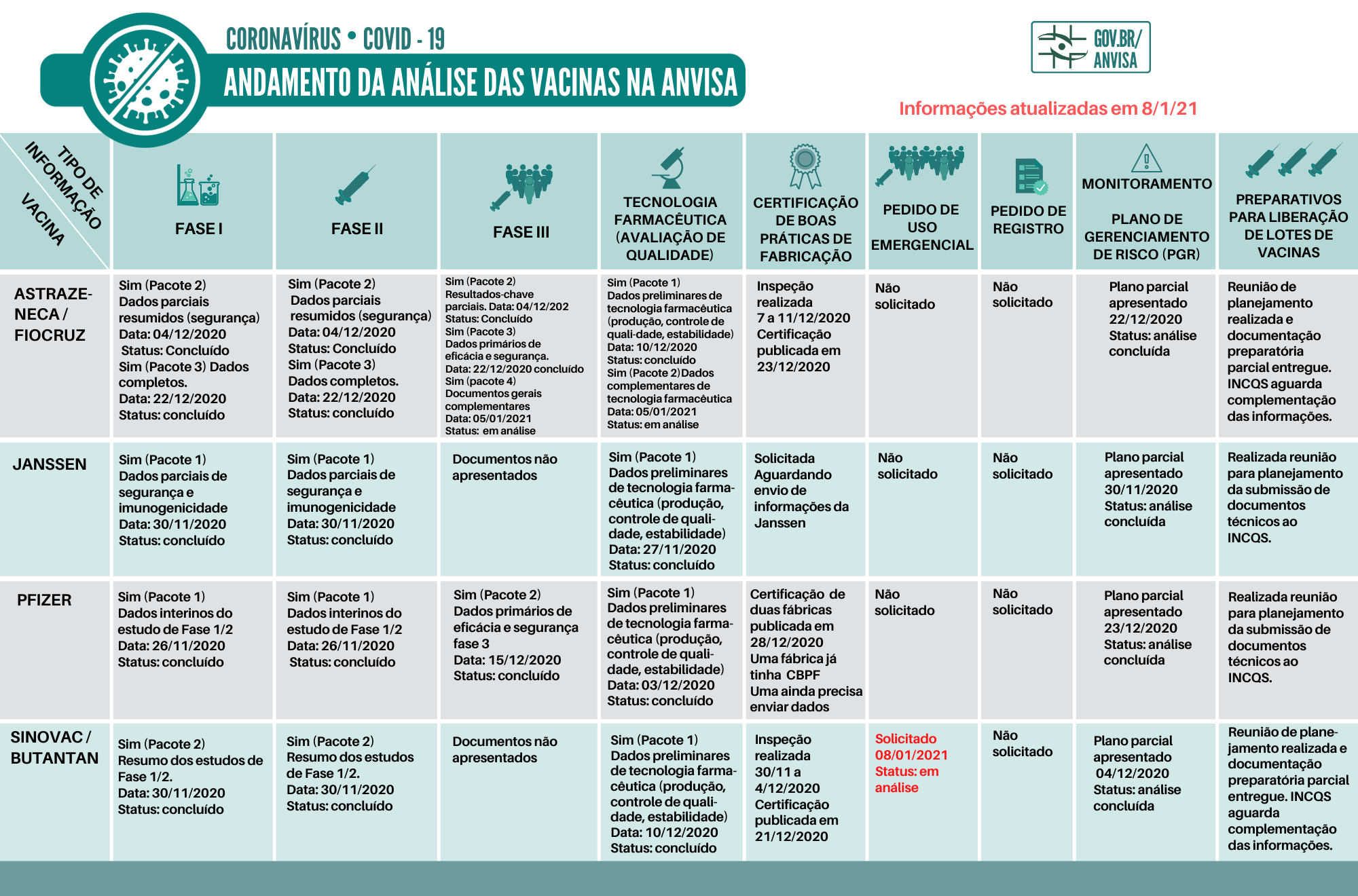
Al momento, la que se constituye en una gran incógnita es la ANVISA de Brasil. El organismo, que a mediados de diciembre determinó un plazo de 10 días para responder a las solicitudes de vacunas anti COVID-19, aún no otorgó ningún uso de emergencia y se mantiene a la fecha sin autorizaciones. Aunque hoy viernes 8 de enero el Instituto Butantan le elevó el pertinente pedido para la vacuna CoronaVac, de la china Sinovac. La agencia regulatoria consignó que se encuentra evaluando su aprobación, por lo que la vacuna de Sinovac podría ser la primera en obtener el visto bueno en Brasil. Otra que está en carpeta pero aún no es oficial es la vacuna de AZ que mantiene un convenio con Fiocruz. Ver check list vacunas Brasil al 8/1/21 Ver artículo.
Por último, la vacuna de la norteamericana Moderna podría tomar impulso en función de que hoy viernes fue aprobada por la MHRA del Reino Unido. A estas horas ya estaría en la mira de México y de Chile. Previo a ello, en diciembre, el producto había recibido el respaldo de la FDA. Casi en simultáneo obtuvo el OK de Puerto Rico que la tiene incluida en su plan de vacunación. Ver artículo Reino Unido
La Sputnik V en Latam
En el mapa de América Latina hay otra vacuna que está tomando fuerza en la región. Se trata de la Sputnik V desarrollada por el Centro Nacional Gamaleya de Epidemiología y Microbiología de Rusia. Desde un inicio Argentina se mostró interesada por este producto y de hecho se convirtió en el primer país del continente en aprobarla.
Fue en vísperas de la Noche Buena, cuando -con carácter de emergencia- se le dio el OK a la vacuna, la que fue adquirida de Estado a Estado. El aval llegó directo desde el Ministerio de Salud de la Nación que se apoya en la ley 27.573, ya que la ANMAT sólo tiene injerencia sobre las empresas reguladas. Ver artículo.
Bolivia fue tras sus pasos. Antes de ayer se transformó en el segundo país en América Latina en autorizarla. La AGEMED le otorgó a la Sputnik V el visto bueno, también bajo la modalidad de uso de emergencia, y sin solicitar ensayos clínicos adicionales en el país. Ver artículo.
El mapa de las vacunas COVID-19 en Latam, informe de Pharmabiz. #Vacunas #COVID19 #Laboratorios #AgenciasRegulatorias #Latam #Farma #Pharmabiz