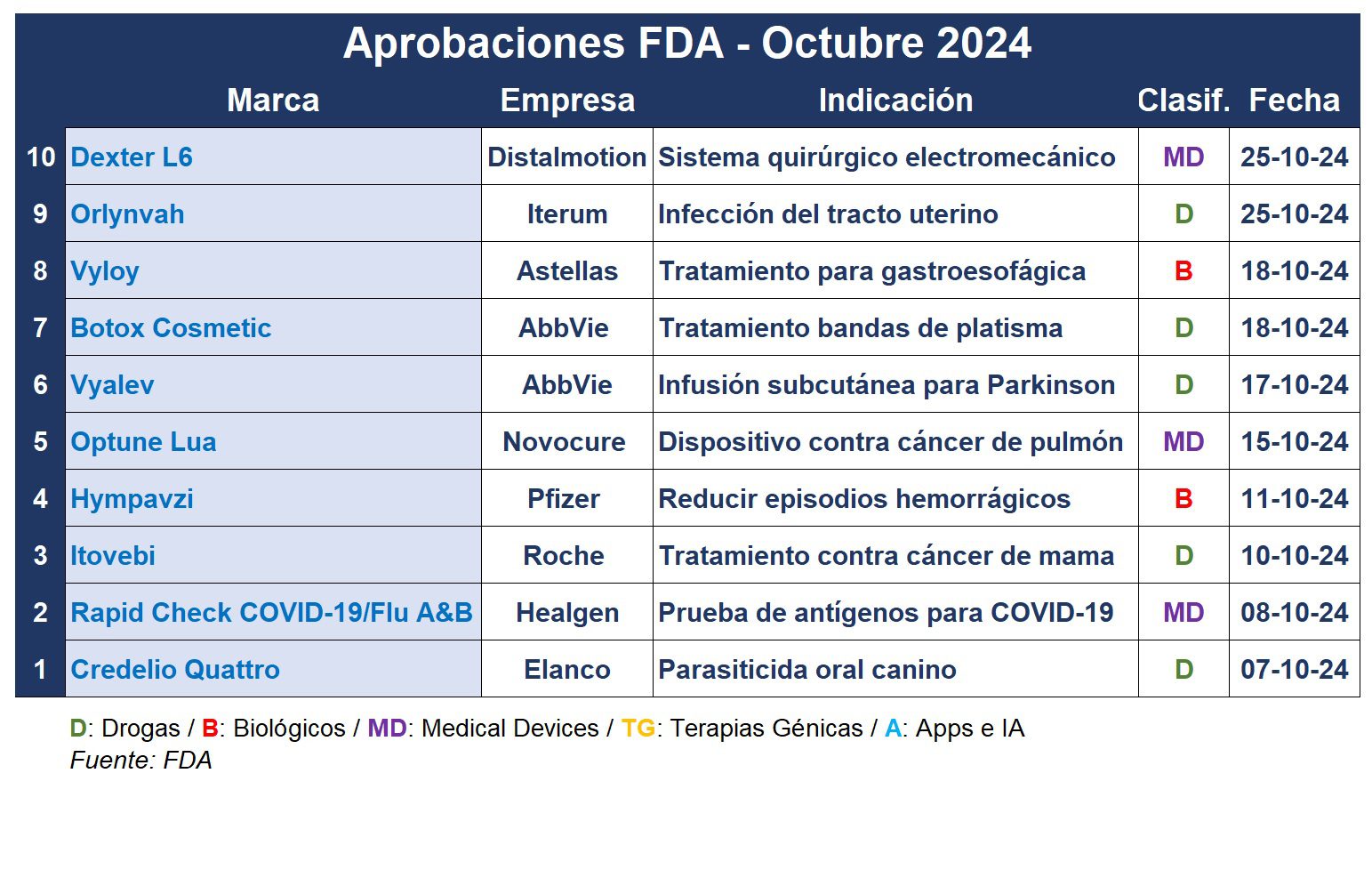
El décimo mes del 2024 cerró con una nutrida lista de aprobaciones de la FDA. Entre las mismas se destaca un tratamiento para la hemofilia A o B, un sistema quirúrgico electromecánico, y tratamientos oncológicos.
Octubre estuvo a todo ritmo para la FDA. Durante el mes cerrado, el organismo regulatorio otorgó diversos avales tales como el de Itovebi, a base de inavolisib, de la suiza Roche. En conjunto con palbociclib y fulvestrant, se convierte en la primera terapia dirigida del laboratorio suizo aprobada para personas con la enfermedad HR positiva, el subtipo de cáncer de mama más prevalente. Ver Press Release
A su vez, en el décimo mes del año, la norteamericana Pfizer obtuvo el aval de la FDA para Hympavzi, indicado para prevenir o reducir los episodios hemorrágicos relacionados con la hemofilia A o B en adultos y adolescentes. El producto se constituye en el primer tratamiento semanal para pacientes con hemofilia A sin inhibidores del factor VIII o hemofilia B sin inhibidores del factor IX. Ver Press Release
En tanto en octubre, la estadounidense AbbVie recibió una dupla de aprobaciones durante el mes. Primero, el organismo regulador autorizó a Vyalev, una infusión continua de 24 horas que combina foscarbidopa y foslevodopa para tratar la enfermedad de Parkinson. El producto ya se comercializa como Produodopa en otros mercados. Ver FDA aprueba Vyalev
Por otro lado, la FDA sumó una nueva indicación para Botox Cosmetic, que ahora se puede utilizar para tratar bandas de platisma de moderadas a graves que conectan la mandíbula y el cuello. AbbVie destacó que su producto es la primera toxina botulínica indicada para cuatro áreas estéticas y la primera para usar no solo en la cara. Está indicada para las líneas de la frente, líneas del entrecejo, líneas de patas de gallo y ahora las bandas de platisma. Ver Press Release
Además Vyloy, de la japonesa Astellas, se convirtió en el primer producto anti-CLDN18.2 aprobado en EE.UU como terapia de primera línea para adultos con adenocarcinoma de unión gástrica o gastroesofágica localmente avanzado irresecable o metastásico del factor de crecimiento epidérmico humano 2 (HER2) negativo cuyos tumores son CLDN18.2 positivos. Ver FDA aprueba Vyloy
En octubre, la FDA aprobó el test de COVID y gripe Healgen Rapid Check COVID-19/Flu A&B de la norteamericana Healgen. Esta resulta la primera prueba de antígenos combinada de venta libre, la que utiliza una muestra de hisopado nasal para brindar resultados en el hogar en 15 minutos para COVID-19 e influenza. Ver FDA aprueba Healgen
Credelio Quattro de la norteamericana Elanco también recibió el visto bueno. Así, estas tabletas masticables se constituyen en el parasiticida oral canino con la protección más amplia del mercado, que protege contra pulgas, garrapatas, gusanos del corazón y los tres parásitos intestinales peligrosos: ascárides, anquilostomas y tenias. Ver FDA aprueba Credelio Quattro
La suiza Novocure consiguió el aval de la FDA para Optune Lua. Indicado para el cáncer de pulmón de células no pequeñas metastásico, el dispositivo portátil administra campos eléctricos de tratamiento de tumores, que alteran la capacidad de las células cancerosas para crecer y dividirse. Ver Press Release
Por su parte, la irlandesa Iterum Therapeutics obtuvo su primera luz verde de la FDA. El OK fue para Orlynvah, un antibiótico oral para tratar infecciones no complicadas del tracto urinario causadas por E. coli, Klebsiella pneumoniae o Proteus mirabilis en mujeres adultas. Ver FDA aprueba Orlynvah
Por último este octubre, la FDA avaló el sistema Dexter L6 de la suiza Distalmotion. Este es un sistema quirúrgico electromecánico destinado a reparar hernias inguinales mediante procedimientos mínimamente invasivos utilizando instrumentos endoscópicos quirúrgicos de alta precisión. Ver Press Release