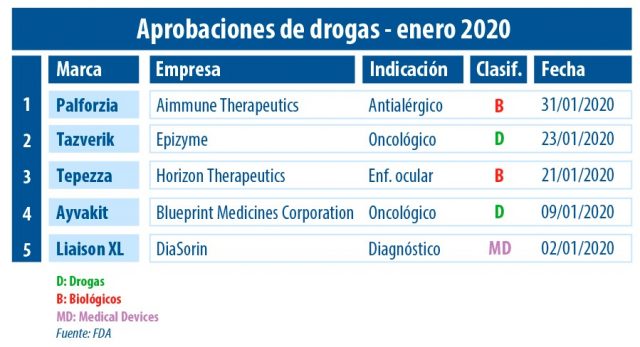
En este arranque del año, la FDA le dio luz verde a un cuarteto de nuevas moléculas, de las cuales dos de ellas fueron productos pertenecientes al segmento de Onco. Además, el organismo le levantó el pulgar a un medical device.
El primer mes del 2020 llegó a su fin y el equipo periodístico de Pharmabiz llevó a cabo un relevamiento de las principales moléculas y dispositivos médicos aprobados por la FDA.
La agencia regulatoria le levantó el pulgar al oncológico Ayvakit de la norteamericana Blueprint Medicines Corporation. El mismo está indicado para el tratamiento de adultos con tumores del estroma gastrointestinal (GIST) no estirpables o metastásicos. Ver artículo.
En tanto, otro oncológico que recibió el aval del organismo fue Tazverik bajo el sello de la norteamericana Epizyme. El medicamento fue desarrollado para el sarcoma epitelioide en adultos y en jóvenes de 16 años o más con metástasis. Ver artículo.
Durante enero, la FDA le dio luz verde también a Tepezza, un biológico de Horizon Therapeutics, dirigido a la enfermedad ocular tiroidea. Esta terapia se constituye como la primera indicada para esta rara condición en la que los músculos del ojo se inflaman y, como resultado, los globos oculares se abultan hacia afuera. Ver artículo.
Asimismo, al filo del final del mes el biológico Paforzia recibió la venia del organismo. Se trata de un antialérgico de la norteamericana Aimmune Therapeutics enfocado en mitigar las reacciones alérgicas, incluida la anafilaxia, provocadas por la exposición al maní. Se constituye como la primera droga para tratar a niños de 4 a 17 años con esta condición. Ver press release.
Dentro del segmento de medical devices, la agencia autorizó a Liaison XL de la italiana DiaSorin, un dispositivo que apunta a detectar anticuerpos del virus de la hepatitis B en la sangre. Ver aprobación.