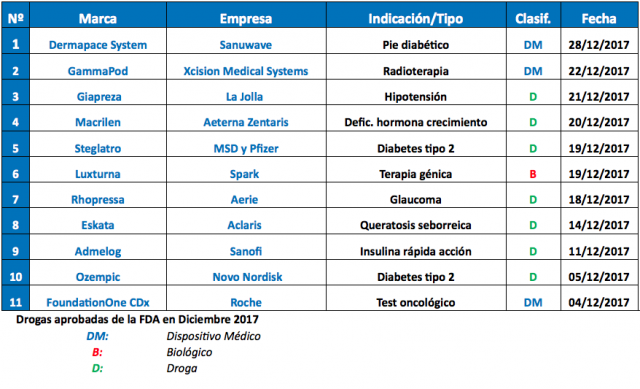
Durante el mes de diciembre la FDA estuvo súper activa en materia de aprobaciones. Por caso, le dio el OK a tres nuevos tratamientos para la diabetes. Los mismos llevan el sello de Novo Nordisk; Pfizer y MSD; y Sanofi.
Pharmabiz realizó un relevamiento de las moléculas que la FDA aprobó durante diciembre. En el último mes del 2017 lo que resaltó sin dudas fueron los tratamientos para la diabetes, que llevaron la delantera.
Entre las compañías que lograron el visto bueno de la FDA, se destacó la danesa Novo Nordisk. Fue con Ozempic, indicado como un complemento de la dieta y el ejercicio para mejorar el control glucémico en adultos con diabetes tipo 2. La multi tenía todas sus fichas puestas en este producto, que competirá con Trulicity, de Eli Lilly. Ver artículo.
El organismo regulatorio le levantó el pulgar a una nueva terapia génica. Se trata de Luxturna, indicada para tratar una forma de pérdida visual hereditaria que puede causar ceguera.
Asimismo, la agencia regulatoria le levantó el pulgar a Steglatro, también para diabetes tipo 2. La marca lleva el sello de las norteamericanas Pfizer y MSD y competirá con Farxiga, de AZ; Invokana de J&J; y con Jardiance de Eli Lilly y B.I.. Ver artículo.
La francesa Sanofi fue otra de las compañías que obtuvo el OK de la FDA para un nuevo producto que apunta a tratar la diabetes tipo 1 y 2. Se trata de Admelog, la primera insulina de rápida acción avalada como “de seguimiento”, que podría llegar a la Argentina en dos años. Ver artículo.
La FDA también le dio autorización a tres nuevos medical devices: un test oncológico de la suiza Roche; un sistema de radioterapia que está bajo el ala de Xcision Medical Systems; y un dispositivo para tratar las úlceras del pie diabético, perteneciente a Sanuwave.
En paralelo, la agencia regulatoria de los Estados Unidos aprobó Luxturna, una nueva terapia génica. El producto, perteneciente a la norteamericana Spark Therapeutics, está indicado para el tratamiento de la distrofia retiniana hereditaria causada por mutaciones en un gen específico, una forma de pérdida visual que puede causar ceguera. Ver artículo.
Hay otros productos disruptivos a los que la FDA le levantó el pulgar durante diciembre. Figuran, por caso, Giapreza -de La Jolla– una inyección para infusión intravenosa indicada para aumentar la presión sanguínea en adultos hipotensos con choque séptico. Ver artículo.
También Macrilen, de Aeterna Zentaris, un medicamento para el diagnóstico de la deficiencia de la hormona de crecimiento en adultos; Rhopressa -de Aerie– que apunta a disminuir la presión intraocular en pacientes con glaucoma; y Eskata -de Aclaris-, una solución tópica para tratar la queratosis seborreica. Ver artículo. Ver artículo.
En materia de devices, la suiza Roche consiguió el sí para un test oncológico. Se trata de FoundationOne CDx, un ensayo integral de perfil genómico tumoral, que proporciona un listado de medicamentos aprobados asociados para identificar cuál es el tratamiento adecuado en cada caso. Ver artículo.
La FDA también respaldó a GammaPod, un sistema de radioterapia estereotáctica no invasiva, indicado para usarse en el tratamiento del cáncer de mama. La marca está bajo el ala de la norteamericana Xcision Medical Systems. Ver artículo.
Llegando al cierre del mes, el organismo le dio luz verde a Dermapace System, el primer dispositivo de onda de choque destinado a tratar las úlceras del pie diabético. El device lleva el sello de la norteamericana Sanuwave. Ver press release.