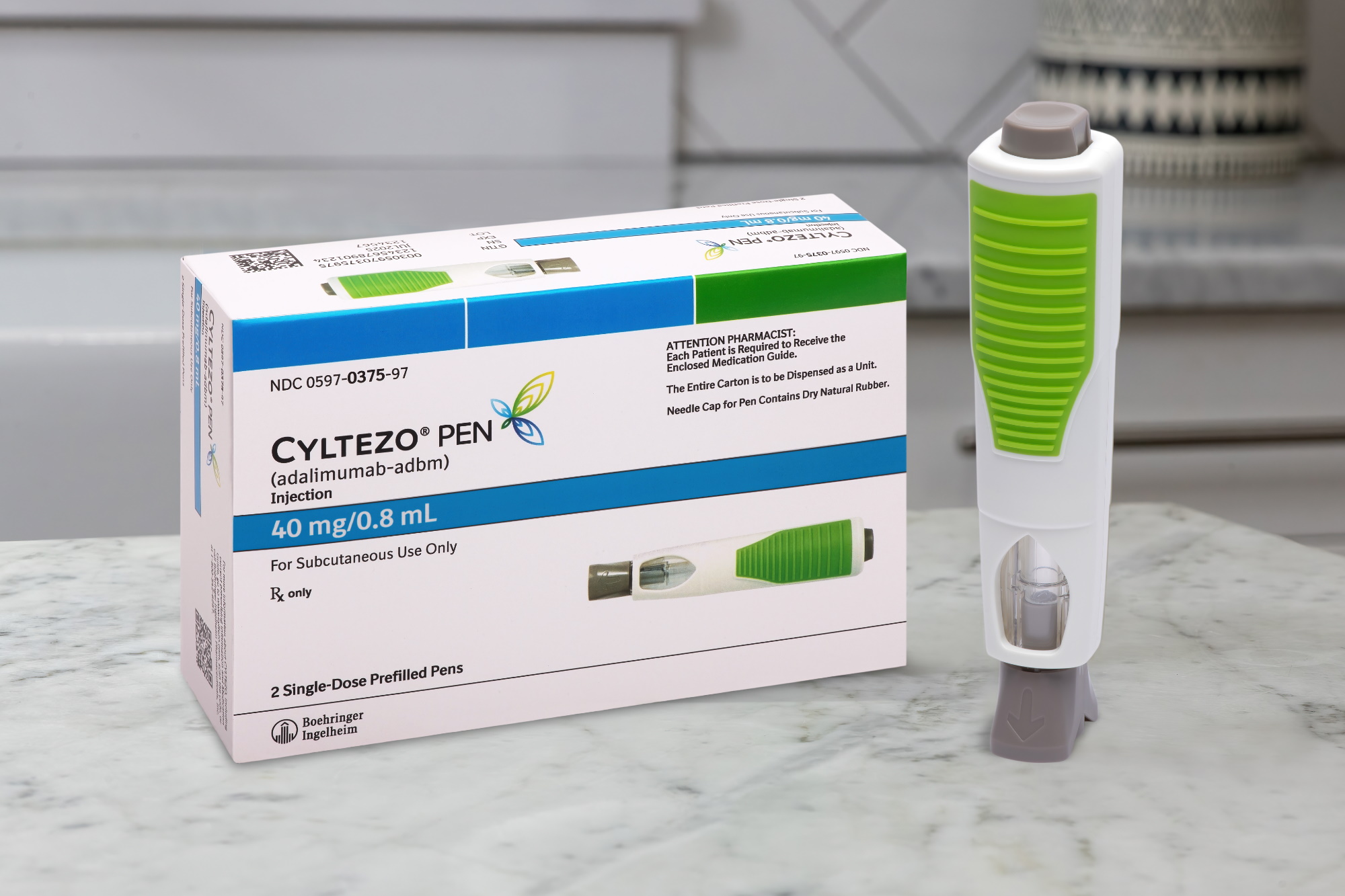
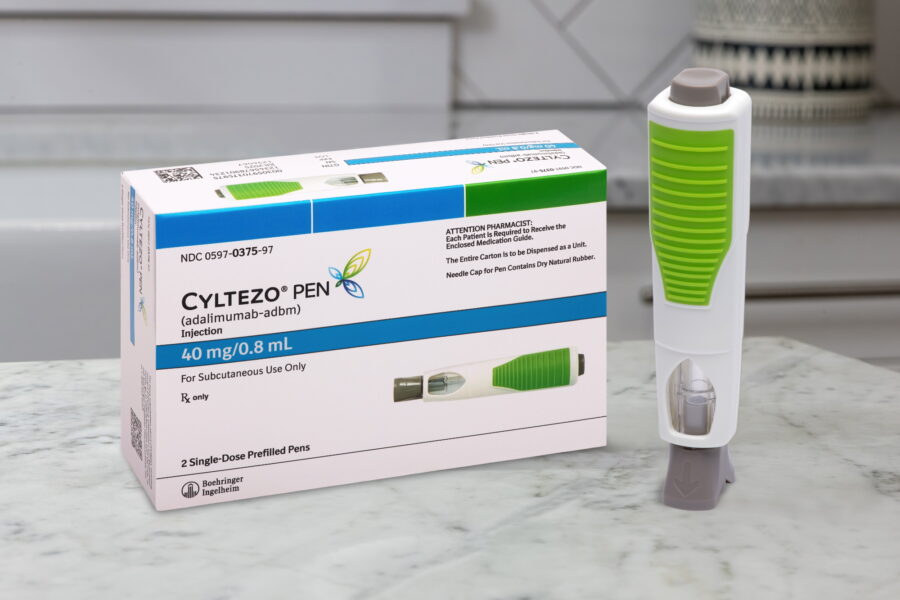
La FDA aprobó hoy el segundo biosimilar en versión pen de Humira, de la norteamericana AbbVie. Se trata de Cyltezo, de la alemana Boehringer Ingelheim, el que había sido avalado en su presentación convencional seis años atrás.
Los alemanes de Boehringer Ingelheim recibieron el OK de la FDA para Cyltezo, su biosimilar de Humira, a base de adalimumab y de la norteamericana AbbVie, seis años atrás. Y ahora sumaron la nueva alternativa de pen autoinyector. Ver Press Release B.I.
Inicialmente, en el 2017, Cyltezo había sido avalado en la presentación de jeringa precargada, e indicado para múltiples enfermedades inflamatorias crónicas como el artritis reumatoide, psoriasis y la enfermedad de Crohn. En esta categoría, figuran también Hyrimoz, de la suiza Sandoz; Hadlima, de la estadounidense MSD; Abrilada, de la norteamericana Pfizer; Hulio, de la norteamericana Mylan; Yusimry, de la estadounidense Coherus; e Idacio, de la alemana Fresenius Kabi. Ver artículo Cyltezo 2017.
En tanto, con su nueva presentación pen, Cyltezo surge como una segunda alternativa. La primera que obtuvo el OK fue Amjevita, de la norteamericana Amgen, en el 2016. Cabe aclarar que, de todos modos, la lapicera subcutánea Humira conserva un diferencial: Abbvie actualizó la formulación hacia una de alta concentración, es decir, que en menor volumen tiene la misma cantidad de droga activa.
De acuerdo con B.I., Cyltezo Pen precargado de 40 mg/0,8 ml estará disponible en Estados Unidos en opciones de dos, cuatro y seis paquetes desde el 1 de julio de 2023. El producto requiere un proceso de activación que consta de tres pasos con un solo botón, 100% de visibilidad del medicamento y una aguja protegida. Está certificado por la Arthritis Foundation como un producto de «facilidad de uso».
“La aprobación de la FDA de Cyltezo Pen es una gran noticia para los pacientes que viven con enfermedades inflamatorias crónicas y que pueden preferir administrar la medicación necesaria para controlar sus afecciones a través de un autoinyector”, señaló Stephen Pagnotta, director ejecutivo y líder comercial de biosimilares en la corporación.