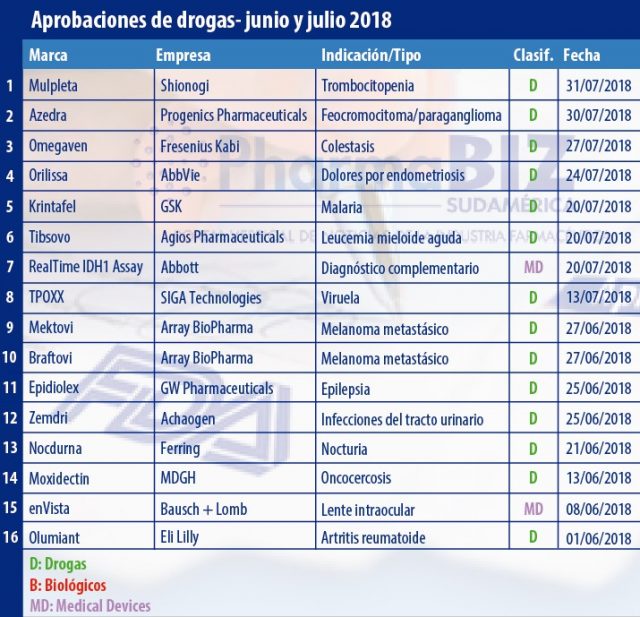
Durante los meses de junio y julio la FDA le dio el visto bueno a más de una docena de medicamentos. En este bimestre los oncológicos volvieron a dar la nota. La agencia le dio luz verde a Braftovi y Mektovi, de Array BioPharma; y a Tibsovo, de Agios Pharmaceuticals.
Pharmabiz realizó un análisis de las aprobaciones otorgadas por la FDA durante junio y julio.
En el bimestre que cerró, cuatro de los OKs del organismo fueron para oncológicos. Por caso, la agencia le levantó el pulgar a Braftovi y Mektovi, ambos de la biotecnológica Array BioPharma, indicados para el tratamiento del melanoma metastásico con cierto tipo de anomalía genética.
También obtuvo luz verde Tibsovo, un nuevo medicamento para leucemia mieloide aguda recurrente o refractaria con una determinada mutación genética. El producto, de la firma Agios Pharmaceuticals, fue avalado para utilizarse en conjunto con un diagnóstico complementario para detectar este tipo de mutaciones, que también recibió el OK del organismo. Es el device RealTime IDH1 Assay, de la norteamericana Abbott. Ver artículo.
En este período también se destacó el aval de TPOXX, de SIGA Technologies, el primer medicamento para la viruela, que aunque fue erradicada en los ’80 se considera que podría ser utilizada como arma biológica.
La agencia aprobó a su vez al oncológico Azedra, de la norteamericana Progenics Pharmaceuticals. El mismo está indicado para adultos y adolescentes con tumores raros de la glándula suprarrenal -feocromocitoma o paraganglioma- que no se pueden extirpar quirúrgicamente.
Otra molécula que consiguió el visto bueno de la FDA fue Olumiant, desarrollada por la norteamericana Eli Lilly junto con la biotecnológica Incyte Corporation. El medicamento, que fue lanzado en la Argentina durante julio, está indicado para adultos con artritis reumatoide moderada o severamente activa. Ver artículo.Ver artículo.
El organismo le levantó el pulgar a dos productos para enfermedades parasitarias. Fueron Krintafel, de la británica GSK, indicado para prevenir recaídas de malaria; y Moxidectin, de la australiana MDGH, para el tratamiento de la oncocercosis.
El laboratorio Abbvie también estuvo en la lista de los aprobados en el bimestre. La multi alcanzó el OK para Orilissa, el primer tratamiento oral indicado para mujeres con dolores causados por la endometriosis. El producto comenzaría a comercializarse en los Estados Unidos a partir de agosto de este 2018. Ver artículo.
Y la viruela sorpresivamente volvió a la escena en esta era. Fue porque la FDA avaló a TPOXX, de SIGA Technologies. Se trata del primer medicamento para esta enfermedad que había sido erradicada en la década del ’80, aunque a través de su correspondiente vacuna. Sin embargo, el organismo aclaró que en la actualidad la viruela podría ser utilizada como arma biológica. Ver artículo.
La agencia también aprobó Epidiolex, de la británica GW Pharmaceuticals. Es el primer jarabe en base a un derivado del cannabidiol en ser avalado por la FDA. Está indicado para tratar las convulsiones causadas por dos formas raras y graves de epilepsia.
Asimismo, la agencia le levantó el pulgar a Krintafel, de la británica GSK. El producto está indicado para prevenir recaídas de malaria causadas por el parásito plasmodium vivax, y fue desarrollado en conjunto con la ONG suiza Medicines for Malaria Venture. Ver artículo.
En sintonía, también recibió el visto bueno Moxidectin, para una enfermedad parasitaria tropical, la oncocercosis. El medicamento lleva el sello de la australiana MDGH, una organización sin fines de lucro enfocada en enfermedades desatendidas. Ver artículo.
A su vez la agencia regulatoria aprobó Epidiolex, de la británica GW Pharmaceuticals. Es el primer jarabe formulado en base a un derivado del cannabidiol que recibe el OK del organismo. Está indicado para tratar las convulsiones causadas por dos formas raras y graves de epilepsia. Ver artículo.
En tanto, la suiza Ferring consiguió el aval para Nocdurna para el tratamiento de la nocturia en adultos debido a la poliuria nocturna, una enfermedad de los riñones. Y la japonesa Shionogi obtuvo luz verde para Mulpleta para el tratamiento de la trombocitopenia en adultos con enfermedad hepática crónica. Ver artículo.
Mientras que la alemana Fresenius Kabi alcanzó el visto bueno para Omegaven, un inyectable indicado como fuente de calorías y ácidos grasos para niños con colestasis asociada a la nutrición parenteral, PNAC. Y la norteamericana Achaogen consiguió el OK para Zemdri, para infecciones complicadas del tracto urinario. Ver artículo.
En la categoría de los medical devices la FDA le levantó el pulgar a enVista, una lente intraocular desarrollada para reemplazar la cristalina natural en adultos. El dispositivo lleva el sello de la oftalmológica Bausch & Lomb.