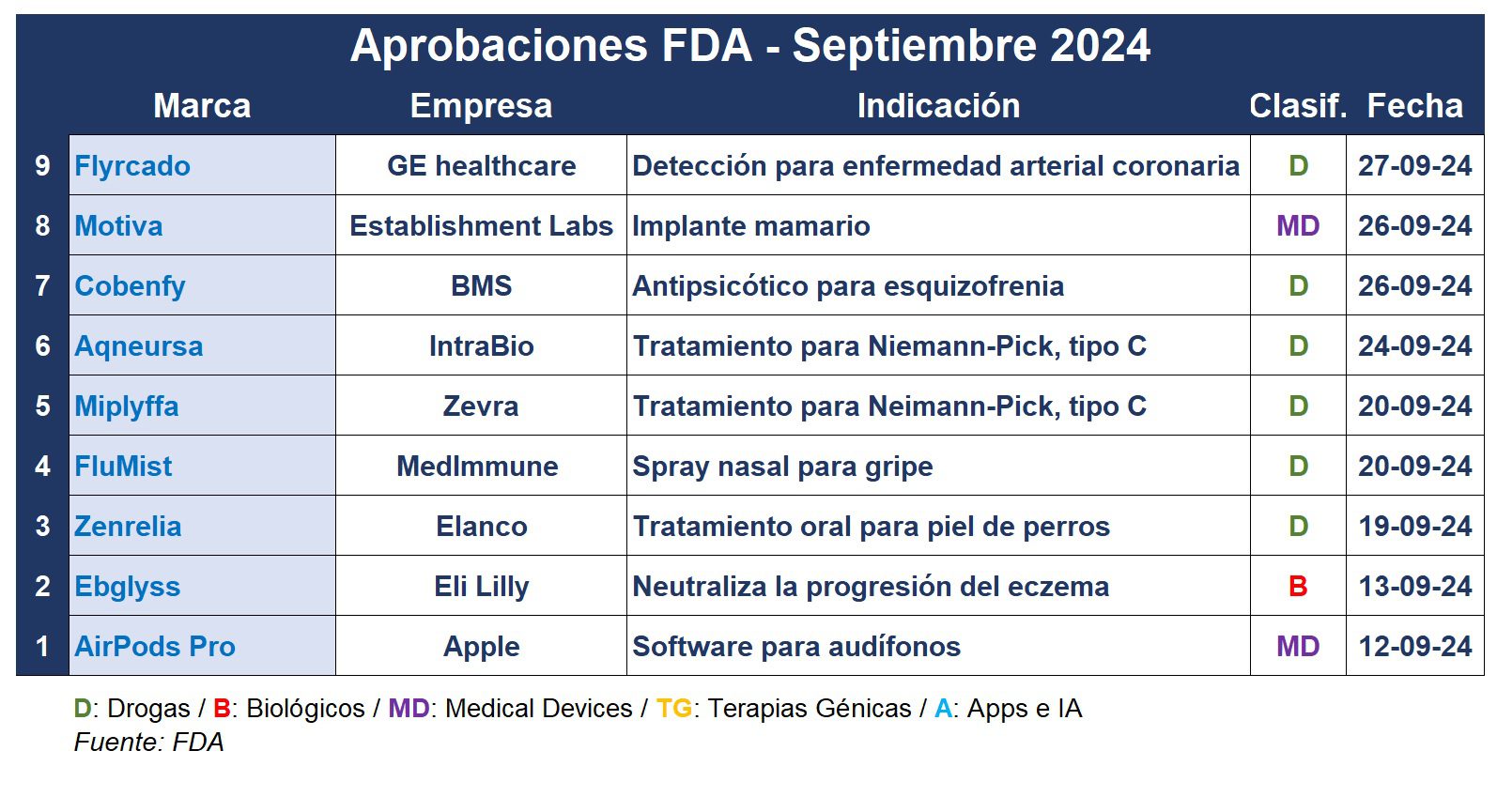
La FDA cerró septiembre con aprobaciones de todo tenor. Entre estas se encuentran las primeras dos moléculas dirigidas a la enfermedad de Niemann-Pick tipo C, un software para audífonos de venta libre, y un producto veterinario.
En septiembre, la FDA aprobó por primera vez una dupla de productos para tratar un trastorno raro conocido como enfermedad de Niemann-Pick tipo C. El primero es Miplyffa de la estadounidense Zevra, el que está indicado para usarse junto con el inhibidor enzimático Zavesca de Janssen. El segundo llegó apenas una semana después, y se trata de Aqneursa de la también norteamericana IntraBio. Ambos se administran por vía oral tres veces al día, y su dosis depende del peso del paciente. Ver FDA OK a Miplyffa | Ver FDA aprueba Aqneursa
La FDA expandió la aprobación con la que FluMist cuenta desde el 2003. El spray nasal, que ahora le pertenece a la británica AstraZeneca, resulta ser la primera vacuna contra la influenza autorizada tanto para la autoadministración como para la administración por un cuidador, sin necesidad de un proveedor de atención médica. El producto está indicado para prevenir la gripe en personas de 2 a 49 años. Ver FDA aprueba FluMist
Otro que recibió la autorización en septiembre fue Ebglyss, un anticuerpo monoclonal del laboratorio estadounidense Eli Lilly para el eczema. Este inyectable indicado para mayores de 12 años, estará disponible en los Estados Unidos en las próximas semanas. Ver FDA aprueba Ebglyss
Y casi al cierre del mes la FDA aprobó la primera terapia para la esquizofrenia en décadas. Cobenfy de la estadounidense BMS es el primer producto antipsicótico aprobado para tratar la esquizofrenia que se dirige a los receptores colinérgicos en lugar de a los receptores de la dopamina. Ver FDA aprueba Cobenfy de BMS
En relación a los medical devices, la FDA autorizó el primer software para audífonos de venta libre. Una vez instalado y personalizado según las necesidades auditivas del usuario, el software permite que los AirPods Pro 2 sirvan como un audífono de venta libre indicado para adultos con discapacidad auditiva leve a moderada. Ver FDA aprueba software auditivo de Apple
A su vez, GE healthcare recibió el aval para Flyrcado. Se trata del primer radiotrazador de imágenes de perfusión miocárdica por tomografía por emisión de positrones (PET) para detectar en adultos con enfermedad de las arterias coronarias conocida o sospechada a fin de evaluar la isquemia miocárdica. El producto se administra mediante inyección intravenosa. Ver FDA le da el OK a Flyrcado de GE
La FDA aprobó la comercialización de los implantes mamarios Motiva rellenos de gel de silicona. Se trata de SmoothSilk Round y SmoothSilk Ergonomix, indicados para el aumento de mamas primario y de revisión. Motiva es una línea de Establishment Labs, una empresa costarricense de tecnología médica enfocada en productos estéticos y de reconstrucción mamaria. Ver Release | Ver Implantes Motiva
Por último, llegó el OK para Zenrelia, un tratamiento para enfermedades de la piel para perros de la norteamericana Elanco. El inmunosupresor oral tiene como objetivo controlar el prurito o picazón asociado con la dermatitis alérgica y controlar la dermatitis atópica en perros de al menos 12 meses. Ver FDA aprueba Zenrelia