Una investigación global del Consorcio Internacional de Periodistas de Investigación puso la lupa sobre la regulación de la tecnología médica. Allí saltó a la luz por caso que en la Argentina, la ANMAT aprobó el ingreso de dispositivos para los que ya se había emitido un recall en EEUU.
El Consorcio Internacional de Periodistas de Investigación -ICIJ por sus siglas en inglés- ya había saltado a la tapa en el 2015 con la famosa investigación de los Panama Papers.
Pero ahora puso la lupa en otro tema en el que los que subieron a primer plano son los organismos regulatorios de medicamentos y tecnología médica de cada país. A dicha investigación la dieron en llamar The Implant Files, se trata de un informe global que puso la lupa en los medical devices y sus minucias.
Así se mostró por caso, que en los Estados Unidos y otros países se aprobaron dispositivos médicos que en los últimos 10 años fueron vinculados a más de 5.4 millones de fallas. Ver informe.
En ese contexto, periodistas argentinos (*) que formaron parte del equipo del ICIJ observaron en primer lugar que el país no cuenta con cifras oficiales sobre la cantidad de prótesis y dispositivos médicos que debieron ser retirados o corregidos en el mercado.
El consorcio de periodistas confrontó los datos de la FDA con los de la Aduana a raíz de que el organismo regulatorio local no contaba con información pública al respecto. Además, los periodistas detectaron que distintas compañías debieron retirar sus productos y la ANMAT nunca lo comunicó.
De modo que los periodistas locales resolvieron cruzar datos públicos de la FDA con los registros de importaciones de la Aduana Argentina y documentos que fueron aportados por la ANMAT y por las empresas importadoras. Así saltaron a la luz dos cuestiones claves. Por un lado, que las autoridades argentinas aprobaron el ingreso al país de dispositivos que ya habían sido retirados en los Estados Unidos; y por otro que en al menos 13 episodios, distintas compañías debieron retirar sus productos o corregirlos y que el organismo local nunca dio a conocer estas decisiones. Ver artículo Perfil.
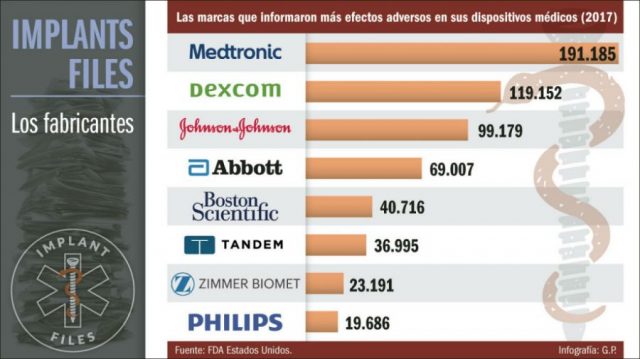
Algunas de las categorías que registraron problemas fueron por caso, dispositivos cardiovasculares, bombas para el corazón, y equipos de diagnóstico o cirugía. Los mismos pertenecen a las principales multis del sector como Medtronic, J&J, General Electric, Philips y Abbott.
Asimismo, Perfil consigna que la regulación de los devices médicos en la Argentina sigue una lógica que establece que si los países “de alta vigilancia”, como los europeos, Estados Unidos, Australia y Japón, autorizan los productos la aprobación local es casi automática. Sin embargo, en el 2013 y tal como lo había publicado Pharmabiz, la ANMAT había establecido nuevos requisitos para la inscripción de productos de tecnología médica y había eliminado el concepto de “países de alta vigilancia sanitaria” incorporando la posibilidad de analizar la pertinencia de que cualquiera de dichos dispositivos provenientes del exterior fuera registrado y comercializado en la Argentina. Ver artículo.
La decisión había llegado luego de un emblemático caso: el de los implantes de mama franceses marca PIP que generaron tantas controversias entre las consumidoras galas y también entre las locales. La ANMAT los prohibió en abril de 2010, poco después de que lo hiciera la agencia regulatoria francesa. Ver Artículo. Ver Disposición.
(*) El equipo argentino del Consorcio Internacional de Periodismo de Investigación que participó de The Implant Files está integrado por Emilia Delfino (Perfil) Mariel Fitz Patrick (Infobae); Sandra Crucianelli (Perfil); Maia Jastreblansky, Iván Ruiz y Ricardo Bron (La Nación).
















